Transaminase (ATA)
Enzyme: Sie sind makromolekulare biologische Katalysatoren; die meisten Enzyme sind Proteine.
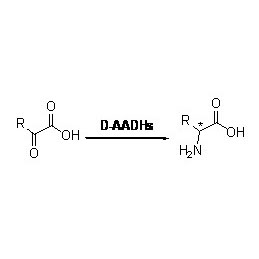
Transaminasen: Eine Enzymklasse, die die Übertragung von Aminogruppen zwischen Aminosäuren und Ketosäuren katalysiert. Transaminasen sind wichtige biologische Enzyme in der asymmetrischen Synthese und der Racematspaltung chiraler Amine.
Aminotransferasen lassen sich anhand ihrer Sequenz und Struktur in vier Klassen einteilen: I, II, III und IV. ω-Aminotransferasen gehören zur Klasse II der Transaminasen und werden häufig zur Herstellung chiraler Amine und unnatürlicher Aminosäuren, wie z. B. β-Aminosäuren, verwendet.
ω-Aminotransferasen: In den meisten Fällen bezeichnet ω-Transaminase eine Klasse von Enzymen, die Ammoniak-Transferreaktionen katalytisch katalysieren, ohne dass α-Aminosäure als Substrat oder Produkt dient.
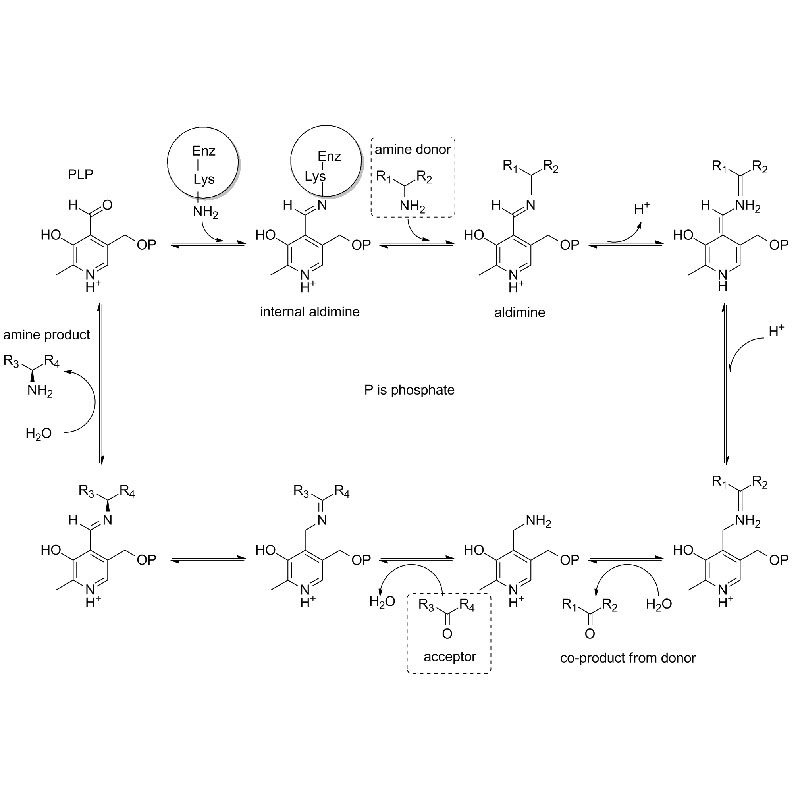
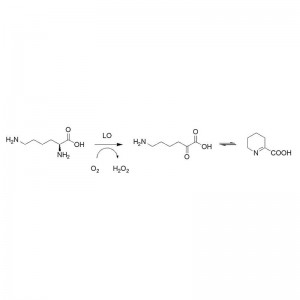
Katalytischer Mechanismus:
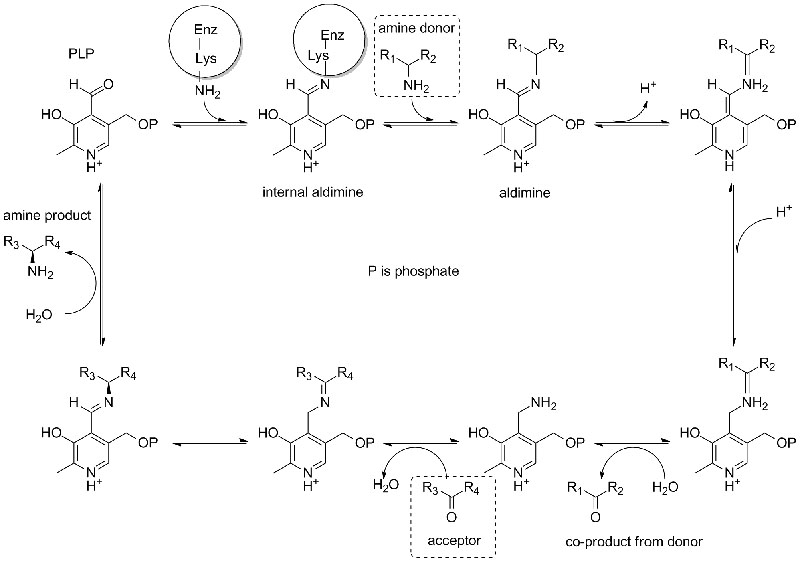
| Enzyme | Produktcode | Produktcode |
| Enzympulver | ES-ATA-101 bis ES-ATA-165 | Eine Packung mit 65 ω-Transaminasen, je 50 mg, 65 Stück à 50 mg oder andere Menge |
| Screening-Kit (SynKit) | ES-ATA-6500 | Eine Packung mit 65 ω-Transaminasen, je 1 mg (65 Stück * 1 mg/Stück) |
★ Hohe Substratspezifität.
★ Starke chirale Selektivität.
★ Hohe Umwandlungseffizienz.
★ Weniger Nebenprodukte.
★ Milde Reaktionsbedingungen.
★ Umweltfreundlich.
➢ Aufgrund der Substratspezifität sollte ein Enzym-Screening für spezifische Substrate durchgeführt werden, um ein Enzym zu erhalten, das das Zielsubstrat mit der besten katalytischen Wirkung katalysiert.
➢ Vermeiden Sie den Kontakt mit extremen Bedingungen wie: hohen Temperaturen, hohem/niedrigem pH-Wert und organischen Lösungsmitteln in hoher Konzentration.
➢ Normalerweise sollte das Reaktionssystem Substrat, Pufferlösung, Aminodonor (wie Aminosäuren und 1-Phenylethylamin) oder Rezeptor (wie Ketosäuren), Coenzym (PLP) und Cosolvens (wie DMSO) enthalten.
➢ ATA sollte erst zuletzt in das Reaktionssystem gegeben werden, nachdem pH-Wert und Temperatur auf die Reaktionsbedingungen eingestellt wurden.
➢ Alle Arten von ATA weisen unterschiedliche optimale Reaktionsbedingungen auf, daher sollte jede von ihnen einzeln weiter untersucht werden.
Beispiel 1 (Synthese von Sitagliptin, asymmetrische Synthese)(1):
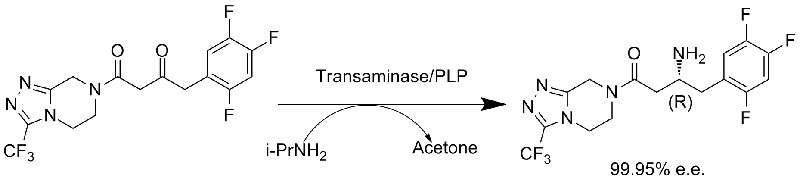
Beispiel 2 (Mexiletin, Kombination aus kinetischer Racematspaltung und asymmetrischer Synthese)(2):
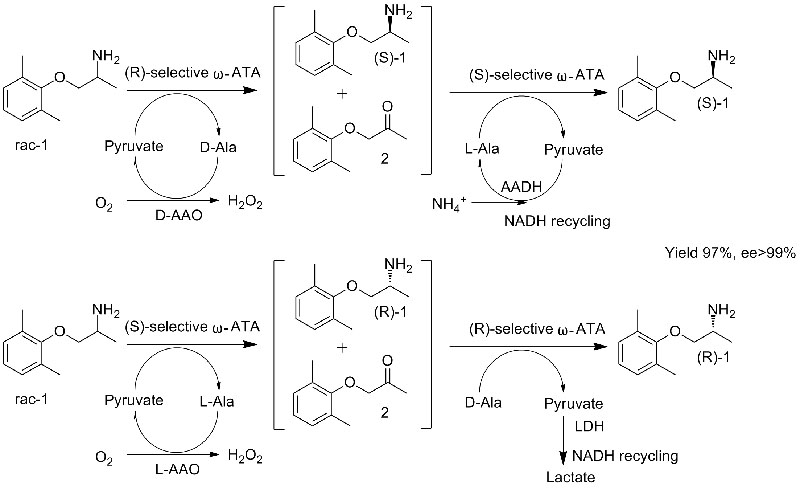
1 Savile CK, Janey JM, Mundorff EC, et al. Science, 2010, 329(16), 305-309.
2 Koszelewski D, Pressnitz D, Clay D, et al. Organische Briefe, 2009,11(21):4810-4812.