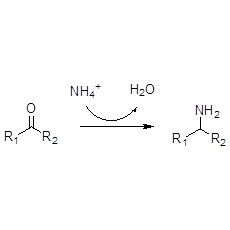
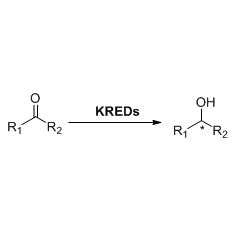
En-Reduktase (ERED)
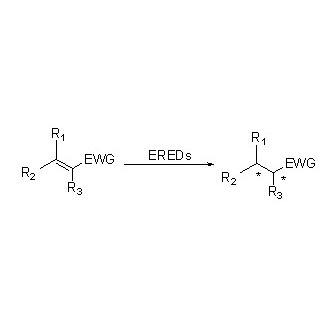
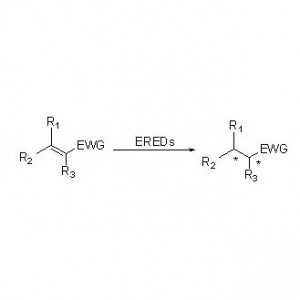
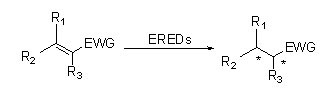
ES-EREDs katalysieren aufgrund ihres breiten Substratspektrums verschiedene Substrattypen. Im Allgemeinen lassen sich die C=C-Doppelbindungen von α,β-ungesättigten Verbindungen mit elektronenabsorbierenden Gruppen (einschließlich Ketonen, Aldehyden, Nitrogruppen, Carbonsäuren, Estern, Anhydriden, Lactonen, Iminen usw.) leicht durch ES-EREDs reduzieren, nicht jedoch nicht-aktivierte Doppelbindungen.
Es gibt 46 verschiedene ERED-Enzymprodukte (Nummerierung ES-ERED-101~ES-ERED-146), die von SyncoZymes entwickelt wurden.
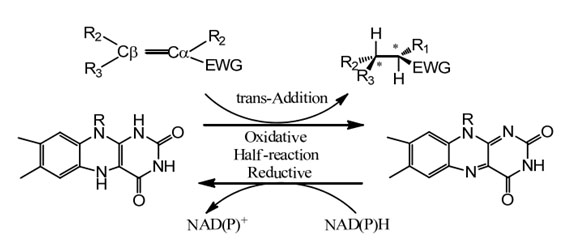
Katalytischer Mechanismus:
| Enzyme | Produktcode | Spezifikation |
| Enzympulver | ES-ERED-101~ ES-ERED-146 | Eine Packung mit 46 Ene-Reduktasen, je 50 mg (46 Stück à 50 mg oder andere Menge) |
| Screening-Kit (SynKit) | ES-ERED-4600 | Eine Packung mit 46 Ene-Reduktasen, je 50 mg (46 Stück à 50 mg oder andere Menge) |
★ Hohe Substratspezifität.
★ Starke chirale Selektivität.
★ Hohe Konversionsrate.
★ Weniger Nebenprodukte.
★ Milde Reaktionsbedingungen.
★ Umweltfreundlich.
★ Hohe Sicherheit.
➢ Normalerweise sollte das Reaktionssystem Substrat, Pufferlösung (optimaler Reaktions-pH-Wert), Coenzyme (NAD(H) oder NADP(H)), Coenzym-Regenerationssystem (z. B. Glucose und Glucose-Dehydrogenase) und ES-ERED umfassen.
➢ Alle ES-EREDs können entweder im oben genannten Reaktionssystem oder mit dem ERED Screening Kit (SynKit ERED) getestet werden.
➢ Alle Arten von ES-EREDs, die verschiedenen optimalen Reaktionsbedingungen entsprechen, sollten einzeln untersucht werden.
➢ Hohe Substrat- oder Produktkonzentrationen können die Aktivität von ES-ERED hemmen. Diese Hemmung lässt sich jedoch durch schrittweise Zugabe des Substrats aufheben.
Beispiel 1 (α,β-ungesättigte Aldehyde oder Ketone)(1):
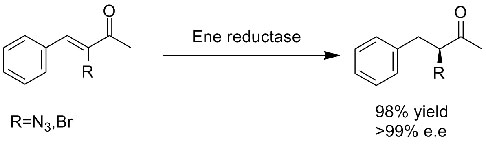
Beispiel 2 (α,β-ungesättigte Carbonsäuren und deren Derivate)(2):
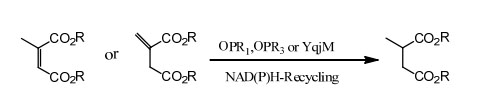
2 Jahre lang unter -20℃ lagern.
Vermeiden Sie jeglichen Kontakt mit extremen Bedingungen wie: hohen Temperaturen, hohem/niedrigem pH-Wert und hochkonzentrierten organischen Lösungsmitteln.
1. Lucidio C, Fardelone J, Augusto R, et al. J.Mol.Catal.B:Enzym., 2004, 29: 41-45.
2. Stueckler C, Hall M, Ehammer H, et al. .Org.Lett, 2007, 9(26): 5409-5411.